分子プロファイリングで、抗がん活性化合物の作用機序を解明
―抗腫瘍活性を有する新規DHODH阻害剤の同定―
国立研究開発法人理化学研究所 環境資源科学研究センター 川谷 誠
Kawatani, M., Aono, H., Shimizu, T., Ohkura, S., Hiranuma, S., Muroi, M., Ogawa, N., Ohishi, T., Ohba, S., Kawada, M., Yamazaki, K., Dan, S., and Osada, H.
Identification of dihydroorotate dehydrogenase inhibitors—indoluidins—that inhibit cancer cell growth.
ACS Chem. Biol. 16: 2570-2580 doi:10.1021/acschembio.1c00625 (2021).
https://pubs.acs.org/doi/10.1021/acschembio.1c00625
国立研究開発法人理化学研究所環境資源科学研究センターの川谷誠専任研究員、長田裕之グループディレクターらの研究グループは、先端モデル動物支援プラットフォーム(AdAMS)の細胞パネルおよびプロテオームによる分子プロファイリングを活用して、新規抗がん剤候補物質の作用を解明することに成功しました。
本研究成果は、がん細胞の複雑な代謝機構を解析する有用なバイオプローブを提供するとともに、新たながん治療法の確立に貢献すると期待できます。
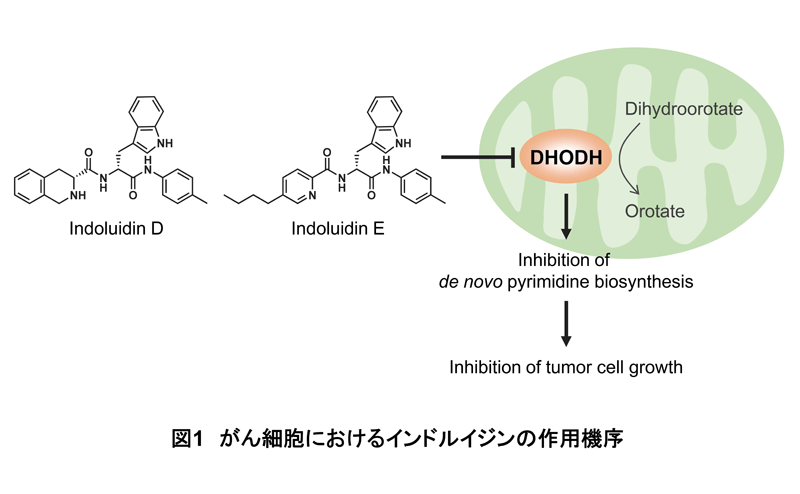
研究グループは、理研天然化合物バンク(RIKEN NPDepo)で保有している化合物ライブラリーから、がん細胞の機能を阻害する化合物を探索し、インドルイジンD(図1)が白血病細胞の分化を50%効果濃度10 nMで強力に誘導し、その後細胞死へ導くことを発見しました。さらに、本化合物はさまざまな固形がん細胞の増殖も50%阻害濃度が数nMから数百nMの範囲で強く阻害することがわかりました。このように、インドルイジンDは強い抗がん活性を有しますが、その作用メカニズムは不明でした。
そこで研究グループは、AdAMSが支援する化合物の分子プロファイリングを活用しました。その結果、細胞パネル増殖解析(JFCR39)およびプロテオーム解析(ChemProteoBase)による分子プロファイリングにおいて、インドルイジンDはdihydroorotate dehydrogenase(DHODH)阻害剤と予測されました。
DHODHは、ピリミジン塩基を新たに生合成する経路に関わる酵素で、ジヒドロオロト酸からオロト酸への反応を触媒します。無制限に増殖するがん細胞では、本生合成経路の活性が亢進しています。近年、DHODHはがん細胞において、核酸合成のみならず、シグナル伝達やエネルギー代謝、転写制御にも関与していることが明らかになり、がんの治療標的として期待されています。
実際、上記の予測どおり、インドルイジンDはDHODHの酵素活性を50%阻害濃度210 nMで阻害し、その結果、白血病細胞の分化誘導や固形がん細胞の増殖阻害を導くことがわかりました(図1)。さらに、活性や物性の向上を目的に合成したインドルイジンE(図1)は、ヒト肺がんモデルマウスにおいて、腫瘍の増大をおよそ80%抑制し、顕著な抗腫瘍効果を示すことが明らかになりました。
DHODHは、がんだけでなく、関節リウマチや多発性硬化症などの自己免疫疾患に対しても有望な創薬標的です。さらに最近では、新型コロナウイルス感染症(COVID-19)の新たな治療標的としても注目されており、今後インドルイジンの創薬への応用が期待されます。また、JFCR39やChemProteoBaseによる分子プロファイリングは、新規生理活性化合物の標的分子や作用機構を迅速かつ高精度に予測する手法として、ケミカルバイオロジー研究や創薬研究に今後ますます活用されることが期待されます。